Qu’est-ce que la stimulation cérébrale profonde (DBS) pour la maladie de Parkinson ?
La stimulation cérébrale profonde (DBS) n’est pas une cure pour la maladie de Parkinson, mais elle change radicalement la vie de nombreux patients. Imaginez un dispositif miniaturisé, implanté dans le cerveau, qui envoie des impulsions électriques pour calmer les signaux déréglés causant les tremblements, la rigidité et les mouvements involontaires. Ce n’est pas de la science-fiction : c’est une réalité depuis plus de 25 ans. Les premiers implants ont été réalisés dans les années 1990, et depuis, plus de 200 000 systèmes ont été implantés dans le monde. En France, comme dans d’autres pays européens, cette technique est devenue une référence pour les patients dont les médicaments ne suffisent plus.
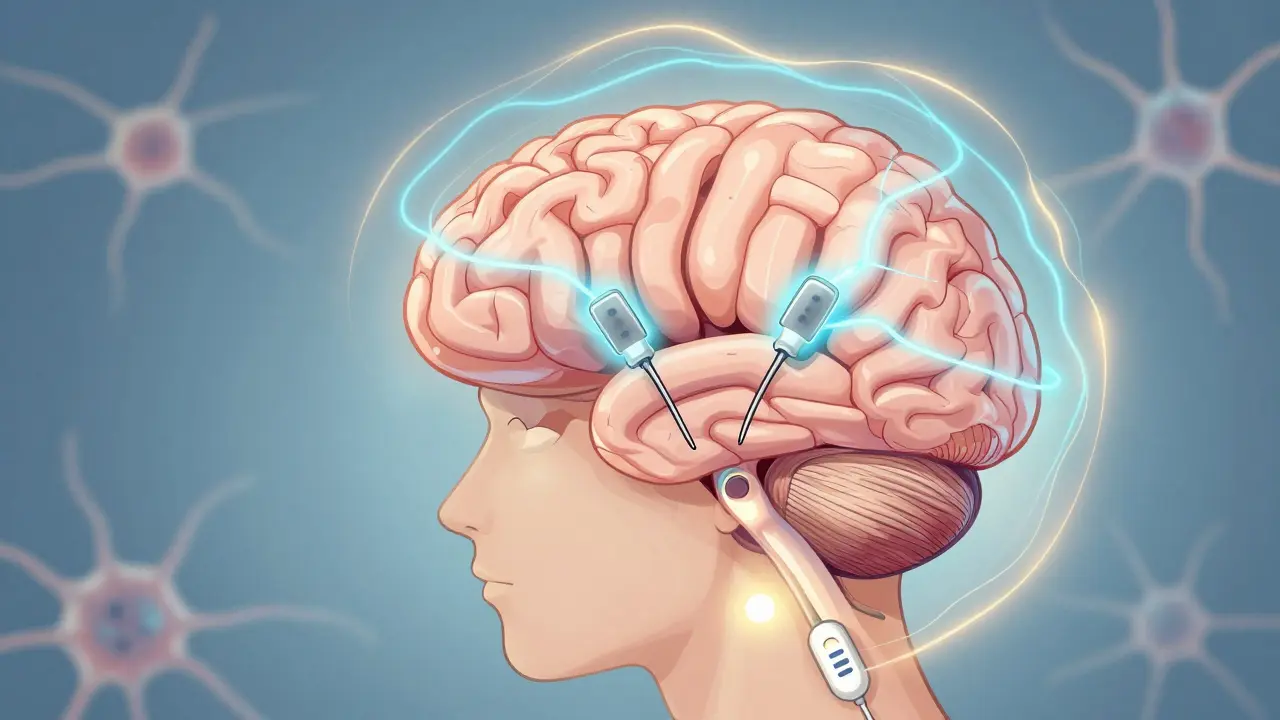
Le principe est simple : des électrodes fines, d’environ 1,27 mm de diamètre, sont placées dans des zones précises du cerveau - généralement le noyau sous-thalamique (STN) ou le globus pallidus interne (GPi). Ces électrodes sont reliées à un générateur d’impulsions (IPG), souvent implanté sous la clavicule ou dans l’abdomen. Ce dispositif envoie des impulsions électriques continues, à des fréquences entre 60 et 185 Hz, pour rétablir un fonctionnement plus normal des circuits cérébraux. Les systèmes modernes, comme le Percept™ PC de Medtronic ou le Vercise™ Genus™ de Boston Scientific, vont encore plus loin : ils peuvent enregistrer l’activité cérébrale en temps réel, détecter les oscillations pathologiques (dans la bande bêta, 13-35 Hz), et même ajuster automatiquement la stimulation.
Qui est un bon candidat pour la DBS ?
La DBS ne convient pas à tous les patients atteints de Parkinson. Les critères sont stricts, mais clairs. D’abord, le diagnostic doit être confirmé : il s’agit d’une maladie de Parkinson idiopathique, et non d’une forme atypique comme la paralysie supranucléaire ou la ataxie multisystémique. Ces dernières ne répondent presque pas à la DBS - moins de 10 % de bénéfice contre 60-70 % pour la forme classique.
Ensuite, la réponse au Lévodopa est essentielle. Un patient doit montrer une amélioration d’au moins 30 % de ses symptômes moteurs après prise de Lévodopa, mesurée par l’échelle UPDRS-III. Si le patient ne réagit pas aux médicaments, la DBS ne fera rien. Ce n’est pas un remède miracle : elle ne traite que les symptômes que les médicaments soulagent déjà.
La durée de la maladie doit être d’au moins cinq ans. Ce n’est pas un arbitraire : c’est pour s’assurer que les complications motrices - les « OFF » (périodes où les médicaments ne fonctionnent pas) et les dyskinésies (mouvements involontaires) - sont bien installées et que les médicaments ne suffisent plus. Enfin, la santé cognitive est vérifiée : un score MMSE supérieur à 24/30 ou un MoCA supérieur à 21/30 est requis. Les patients avec troubles de la mémoire, de l’attention ou des fonctions exécutives sont souvent exclus, car la DBS peut les aggraver.
Quels sont les bénéfices réels après l’implantation ?
Les résultats sont spectaculaires pour les bons candidats. Dans l’essai EARLYSTIM publié en 2013 dans le New England Journal of Medicine, les patients ayant reçu la DBS tôt (après 4 ans de maladie) ont vu leurs symptômes moteurs s’améliorer de 23 points sur l’échelle PDQ-39 - contre seulement 12,5 pour ceux qui ont continué les médicaments seuls. Cela signifie une vraie amélioration de la qualité de vie : pouvoir s’habiller seul, marcher sans aide, ou encore dormir sans être réveillé par des contractions musculaires.
Les chiffres sont parlants :
- Les périodes « OFF » sont réduites de 60 à 80 %
- Les dyskinésies diminuent de jusqu’à 80 %
- La dose quotidienne de Lévodopa peut être abaissée de 30 à 50 %
Beaucoup de patients rapportent retrouver leur indépendance. Un homme de 62 ans à Lyon, après son implantation STN, a pu reprendre le vélo après 7 ans d’arrêt. Une femme de 71 ans, qui ne pouvait plus sortir de chez elle à cause des tremblements, a retrouvé le plaisir de faire ses courses. Ces histoires ne sont pas rares - elles sont la norme pour les patients bien sélectionnés.

Les différences entre STN et GPi : quel cible choisir ?
Deux cibles principales existent : le noyau sous-thalamique (STN) et le globus pallidus interne (GPi). Les deux sont efficaces, mais elles n’ont pas les mêmes effets.
Le STN permet une réduction plus importante des médicaments - idéal pour les patients qui souffrent des effets secondaires des traitements oraux. Mais il peut aussi entraîner des troubles cognitifs ou du langage : certains patients ont plus de mal à trouver leurs mots ou à planifier leurs tâches. Sur le forum Parkinson’s Foundation, un utilisateur a écrit : « Mes tremblements ont disparu, mais maintenant, je mets trois fois plus de temps à préparer un repas. »
Le GPi, lui, est plus doux sur les fonctions cognitives. Il est souvent préféré pour les patients avec de fortes dyskinésies ou des antécédents de dépression. Une étude publiée dans Neurology en 2009 a montré que le GPi réduisait les dyskinésies de 70 % contre 46 % pour le STN. Pour les patients avec des symptômes moteurs très marqués, mais peu de troubles cognitifs, le STN reste le choix le plus efficace. Le choix se fait en équipe : neurologue, neurochirurgien, neuropsychologue.
Les risques et les limites de la DBS
La DBS n’est pas sans risques. Le taux d’hémorragie cérébrale est faible - entre 1 % et 3 % - mais c’est un risque grave. Les complications liées aux équipements (infection, déplacement des électrodes, rupture des câbles) touchent 5 à 15 % des patients. Certaines nécessitent une nouvelle intervention chirurgicale.
Le coût est aussi un frein. Aux États-Unis, l’implantation coûte entre 50 000 et 100 000 dollars. En Europe, les systèmes sont pris en charge par la sécurité sociale, mais le processus d’approbation peut prendre des mois. De plus, les systèmes non rechargeables doivent être remplacés tous les 3 à 5 ans. Même avec les batteries rechargeables (9 à 15 ans de durée), il faut des visites régulières pour ajuster la stimulation - parfois pendant plus d’un an avant d’atteindre le réglage optimal.
Et puis, il y a les attentes mal placées. Beaucoup croient que la DBS arrête la maladie. Elle ne le fait pas. Elle ne traite que les symptômes moteurs responsifs au Lévodopa. Les problèmes de marche, d’équilibre, de parole ou de dépression ne sont pas toujours améliorés. Un patient sur trois rapporte une déception après l’opération parce qu’il pensait que tout irait mieux. La communication avant l’intervention est cruciale.

Comment se déroule le processus de sélection ?
Le parcours ne commence pas par une chirurgie. Il dure entre 3 et 6 mois. Voici les étapes :
- Confirmation du diagnostic de Parkinson idiopathique par un neurologue spécialisé
- Évaluation de la réponse au Lévodopa : test UPDRS-III avant et après prise de médicament
- Évaluation neuropsychologique complète (4 à 6 heures) : mémoire, attention, fonctions exécutives, humeur
- IRM cérébrale haute résolution (3 Tesla minimum) pour localiser les cibles
- Réunion multidisciplinaire : neurologue, neurochirurgien, neuropsychologue, kinésithérapeute
- Discussion avec le patient et la famille : avantages, risques, attentes réalistes
À Lyon, comme dans les grands centres universitaires, cette équipe est souvent composée de 5 à 7 professionnels. Les centres qui font plus de 50 interventions par an ont des taux de complications 20 % plus bas. C’est pourquoi il est crucial de se tourner vers un centre expérimenté.
La DBS : un traitement sous-utilisé
Malgré ses bénéfices prouvés, la DBS est encore trop peu prescrite. Seulement 1 à 5 % des patients éligibles la reçoivent. Pourquoi ? Parce qu’elle est souvent proposée trop tard. Beaucoup de patients passent des années à essayer des médicaments de plus en plus lourds, sans jamais être orientés vers un centre de DBS. Le Parkinson’s Foundation le dit clairement : « Beaucoup de patients ne sont jamais évalués du tout. »
Et pourtant, les données montrent que plus on agit tôt, mieux c’est. L’essai EARLYSTIM a montré que des patients opérés après seulement 4 ans de maladie avaient une meilleure qualité de vie que ceux attendus jusqu’à 7 ans. Un nouveau projet, l’EARLYSTIM-2, teste même la DBS après seulement 3 ans de maladie. L’idée ? Ne pas attendre que la vie devienne insoutenable.
Quel avenir pour la DBS ?
La technologie évolue vite. Le Percept™ PC de Medtronic, approuvé en 2020, est le premier système « boucle fermée » : il ajuste la stimulation en temps réel en fonction de l’activité cérébrale. L’essai INTREPID a montré une amélioration de 27 % des symptômes par rapport aux systèmes classiques.
À l’avenir, la DBS pourrait intégrer des capteurs externes - comme un Apple Watch qui détecte les tremblements - pour envoyer des données en direct au stimulateur. Des recherches explorent aussi son usage pour les symptômes non moteurs : dépression, anxiété, troubles du sommeil. Une étude de 2023 dans The Lancet Neurology montre que les porteurs d’une mutation LRRK2 répondent 15 % mieux à la DBS. Cela ouvre la voie à une médecine personnalisée, basée sur la génétique et la biologie du patient.
Le vrai défi reste d’atteindre ceux qui n’ont pas accès à ces soins. Dans les zones rurales ou les pays à faibles ressources, la DBS reste un luxe. Même en France, les délais d’attente peuvent dépasser un an. La solution ? Former davantage de professionnels, simplifier les protocoles, et surtout, parler plus tôt de la DBS - pas comme une dernière option, mais comme une étape naturelle dans la prise en charge de la maladie de Parkinson.
La DBS peut-elle arrêter la progression de la maladie de Parkinson ?
Non. La stimulation cérébrale profonde ne ralentit ni ne stoppe la progression de la maladie de Parkinson. Elle agit uniquement sur les symptômes moteurs qui répondent déjà au Lévodopa - tremblements, rigidité, lenteur, dyskinésies. Les symptômes non moteurs (troubles de l’équilibre, de la parole, de la mémoire, dépression) ne sont pas toujours améliorés. C’est un traitement symptomatique, pas curatif.
Quelle est la différence entre STN et GPi comme cibles de stimulation ?
Le noyau sous-thalamique (STN) permet une réduction plus importante des médicaments (jusqu’à 50 %), ce qui est avantageux pour les patients souffrant d’effets secondaires du Lévodopa. Cependant, il peut augmenter les risques de troubles cognitifs ou du langage. Le globus pallidus interne (GPi) est plus efficace pour réduire les dyskinésies (70 % contre 46 %) et est plus sûr sur le plan cognitif. Le choix dépend du profil du patient : ses symptômes dominants, son âge, son état cognitif, et ses priorités de vie.
Faut-il être opéré tôt ou attendre que les médicaments échouent ?
Les données récentes suggèrent qu’opérer plus tôt (après 4 à 5 ans de maladie) donne de meilleurs résultats en qualité de vie que d’attendre que les symptômes deviennent sévères. L’essai EARLYSTIM a prouvé que les patients opérés plus tôt avaient une amélioration de la qualité de vie plus marquée. Ne pas attendre que la maladie devienne invalidante est désormais une recommandation des experts. Cela ne signifie pas opérer dès les premiers symptômes, mais plutôt dès que les complications motrices apparaissent malgré un bon traitement médical.
La DBS fonctionne-t-elle pour tous les types de Parkinson ?
Non. La DBS est efficace uniquement pour la maladie de Parkinson idiopathique, qui représente environ 85 % des cas. Elle a peu ou pas d’effet sur les formes atypiques comme la paralysie supranucléaire, la ataxie multisystémique ou le syndrome parkinsonien lié aux médicaments. Ces formes ne répondent pas au Lévodopa, et donc pas à la DBS. Un diagnostic précis est indispensable avant toute évaluation.
Quels sont les effets secondaires courants après l’implantation ?
Les effets secondaires les plus fréquents sont temporaires et liés à l’ajustement de la stimulation : picotements, troubles de l’équilibre, troubles du langage (trouver ses mots), ou changements d’humeur. Certains patients rapportent une baisse de la motivation ou de la capacité à planifier. Ces effets peuvent souvent être corrigés en modifiant les paramètres du stimulateur. Les complications graves - infection, hémorragie, déplacement de l’électrode - sont rares (1 à 5 %), mais nécessitent une prise en charge urgente.
Combien de temps dure l’effet de la DBS ?
Les bénéfices moteurs sont durables. Des études suivent les patients jusqu’à 10 ans après l’implantation et montrent que 85 % conservent une amélioration significative de leurs symptômes. Cependant, la maladie progresse naturellement, et certains symptômes (marche, équilibre) deviennent moins réactifs avec le temps. Le stimulateur doit être régulièrement ajusté, et les piles remplacées tous les 3 à 15 ans selon le type. La DBS n’est pas un traitement unique, mais un outil à entretenir.
Valentin Duricu
mars 20, 2026 AT 00:24Kim Girard
mars 21, 2026 AT 01:31Bernard Chau
mars 21, 2026 AT 02:02Dani Schwander
mars 21, 2026 AT 16:42Cyrille Le Bozec
mars 23, 2026 AT 02:22Léon Kindermans
mars 24, 2026 AT 19:45Marvin Goupy
mars 25, 2026 AT 02:17Jean-Marc Frati
mars 26, 2026 AT 15:12mathilde rollin
mars 27, 2026 AT 16:43nadine deck
mars 28, 2026 AT 21:45cyril le boulaire
mars 30, 2026 AT 16:19Helder Lopes
mars 30, 2026 AT 21:42Guy COURTIEU
avril 1, 2026 AT 14:22